
REGENXBIO informa del Ă©xito de un ensayo clave para el tratamiento de la MPS II
ROCKVILLE, Maryland - REGENXBIO Inc. (NASDAQ: RGNX) ha anunciado hoy los resultados positivos de su ensayo pivotal CAMPSIITE® de RGX-121 para la Mucopolisacaridosis Tipo II (MPS II), también conocida como síndrome de Hunter.
+INFO

Denali Therapeutics está investigando un nuevo tratamiento para el sĂndrome de Hunter
Denali Therapeutics ha desarrollado DNL310, un tratamiento intravenoso semanal en investigación para niños que viven con el síndrome de Hunter. DNL310 está diseñado para administrar la enzima iduronato-2-sulfatasa a través de la barrera hematoencefálica hasta el cerebro.
+INFO
REGENXBIO presenta datos provisionales adicionales del ensayo de fase I/II de RGX-121 para el tratamiento de MPS II (sĂndrome de Hunter)
RGX-111, es una terapia génica única potencial para MPS I, se tolera bien en los dos niveles de dosis, sin efectos adversos graves relacionados con el medicamento.
+INFO

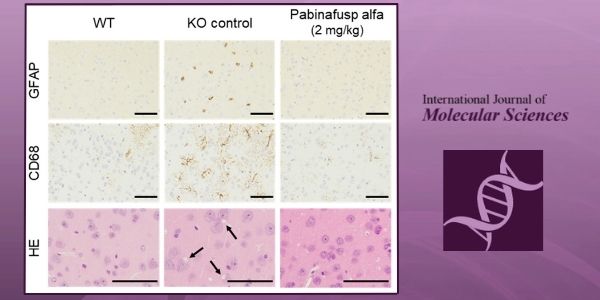
Terapia de reemplazo enzimático con Pabinafusp Alfa para Mucopolisacaridosis II neuronopática
Este artículo resume y actualiza la evidencia clínica y preclínica de la eficacia dual de pabinafusp alfa contra los síntomas somáticos neuronopáticos tanto centrales como periféricos de la MPSII.
+INFO
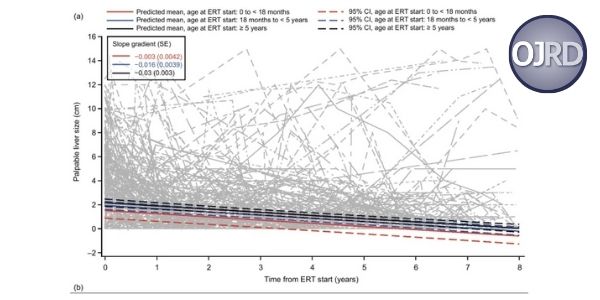
EvaluaciĂłn del tratamiento a largo plazo de los efectos de la idursulfasa intravenosa en pacientes con MPS II
Evaluación del tratamiento a largo plazo de los efectos de la idursulfasa intravenosa en pacientes con Mucopolisacaridosis II (MPS II) usando como modelo estadístico: los datos de la encuesta de resultados de Hunter (HOS).
+INFO

La EMA otorga la designaciĂłn PRIME a JR-141 para el tratamiento de la mucopolisacaridosis tipo II (sĂndrome de Hunter
18 de octubre de 2021 - JCR Pharmaceuticals Co., Ltd. (TSE 4552; presidente: Shin Ashida; "JCR") ha anunciado que la Agencia Europea de Medicamentos (EMA) ha otorgado la designación PRIME al medicamento en investigación para el tratamiento de la mucopolisacaridosis (MPS) II (síndrome de Hunter), JR-141 (pabinafusp alfa).
+INFO
JR-141 (Pabinafusp Alfa) para el SĂndrome de Hunter
Aviso sobre la publicación de evidencia clínica y no clínica en la Revista Internacional de Ciencias Moleculares
+INFO


Takeda comercializará una terapĂa de Ăşltima generaciĂłn para el SĂndrome de Hunter en colaboraciĂłn con JCR Pharmaceuticals.
JR-141 es una terapia potencialmente transformadora diseñada para suministrar, por vía intravenosa, proteínas al cerebro y a los tejidos periféricos para tratar los rasgos neuronopáticos junto con los síntomas somáticos del síndrome de Hunter
+INFO
ActualizaciĂłn de desarrollo clĂnico - Sangamo
Sangamo proporciona una actualización de desarrollo clínico que incluye datos de terapia celular editados por el gen de fase 1/2 Beta talasemia temprana. "Durante los últimos tres años, hemos construido una base sólida para respaldar a la organización clínica de Sangamo"
+INFO


Beca para la Terapia GĂ©nica de Hunter
MPS concedió una beca de 9.000 € al equipo del `Centre de Biotecnologia Animal i Teràpia Gènica de la UAB´ coordinado por la Dra. Fàtima Bosch para el desarrollo de la Terapia Génica de Hunter `Gene Therapy for Muccopolysacharidosis Type II, Hunter Disease'.
+INFO
Contacto
email : info@mpsesp.org
Teléfono : 93 804 09 59 / 692986068
Hogar MPS España (piso de acogida)
Avda. Barcelona nÂş 174 1Âş 2ÂŞ
08700 Igualada (Barcelona)






























